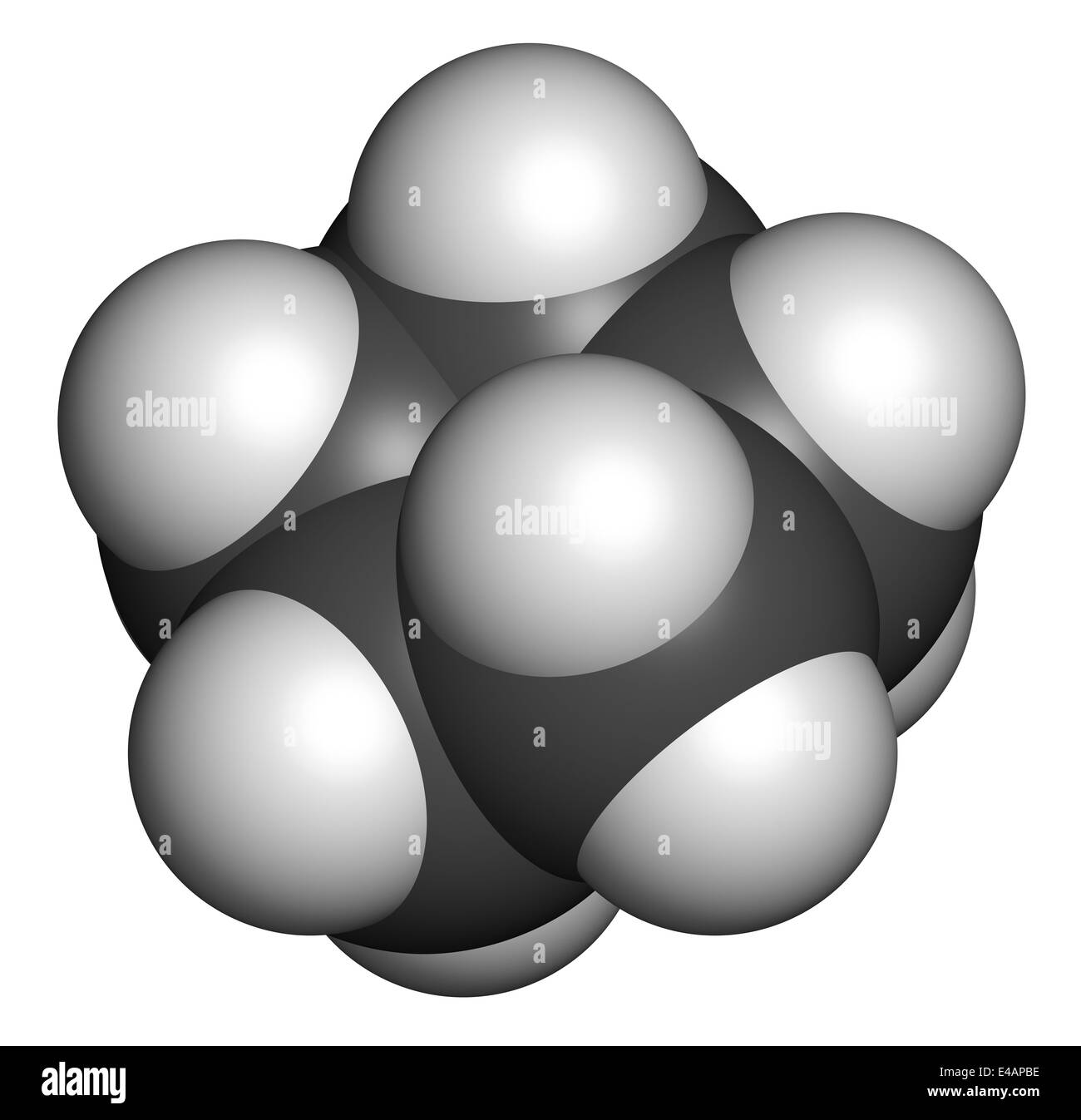
Cyclooctan ist eine organisch-chemische Verbindung, die zur Stoffgruppe der Cycloalkane gehört. Die Verbindung kann in verschiedenen Konformeren auftreten.
Darstellung und Gewinnung
Die Verbindung kann durch eine Hydrierung von 1,5-Cyclooctadien, welches technisch aus 1,3-Butadien erhalten wird, hergestellt werden.
Eigenschaften
Cyclooctan ist eine schwach riechende, farblose Flüssigkeit. Der Siedepunkt liegt bei Normaldruck bei 151,2 °C. Die molare Verdampfungsenthalpie beträgt 43,35 kJ·mol−1. Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T C)) (P in bar, T in K) mit A = 3,98805, B = 1438,687 und C = −63,024 im Temperaturbereich von 369.9 K bis 467,5 K. Die kritischen Größen betragen für die kritische Temperatur 374 °C, für den kritischen Druck 35,6 bar, das kritische Volumen 0,4 l·mol−1 und für die kritische Dichte 2,44 mol·l−1. In fester Phase treten drei polymorphe Kristallformen auf. Das Polymorph III wandelt sich bei −106,6 °C mit einer Umwandlungsenthalpie von 6,306 kJ·mol−1 in das Polymorph II um. Bei −89,4 °C erfolgt dann die Umwandlung von Polymorph II zum Polymorph I mit einer Umwandlungsenthalpie von 0,478 kJ·mol−1. Das Polymorph I schmilzt bei 14,8 °C mit einer Schmelzenthalpie von 2,410 kJ·mol−1. Die Wärmekapazität beträgt bei 25 °C 215,53 J·mol−1·K−1 bzw. 1,92 J·g−1·K−1.
Cyclooctan bildet leicht entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt von 28 °C. Die untere Explosionsgrenze liegt bei 0,95 Vol.‑%. Die Zündtemperatur beträgt 250 °C. Der Stoff fällt somit in die Temperaturklasse T3.
Konformationen
Cyclooctan ist repräsentativ für viele Achterringe. Seine Konformation wurde intensiv computerunterstützt untersucht. Hendrickson bemerkte, dass die „Boat-Chair“-Konformation die stabilste ist, was von Allinger und seinen Mitarbeitern bestätigt wurde. Die „Crown“-Konformation ist weniger stabil.
Weblinks
Einzelnachweise